 뉴스센터
뉴스센터
![[코로나19 과학 리포트 2]_Vol.13 학부생 인턴, 코로나19 최전선의 연구실을 경험하다](https://www.ibs.re.kr:443/dext5data/2021/05/20210514_132917233_56204.jpg)
생명과학 전공 대학생이 본 코로나19 팬데믹 <2>‘팬데믹(Pandemic): 세계적으로 전염병이 대유행하는 상황’ 학부 1학년 때 일반생물학 교과서에서 본 단어를 실제로 체험하게 될 줄은 상상도 못했다. 지난해 3월 세계보건기구(WHO)의 팬데믹 선언은 전공자들에게만 익숙했던 이 단어를 전 세계에서 모르는 사람이 없게 만들었다. 필자는 코로나19 국내 확산 초기 대구의 본가에서 지내며 비대면 수업을 듣고 있어서 사태의 심각성을 직접 느낄 수 있었다. 그러나 다음 학기에 서울에 오니 이번엔 서울이 대구보다 더 많은 확진자가 발생했다. 이 전염병이 특정 지역이 아닌, 전 지구적으로 벗어나기 어려운 문제임을 실감했다. 생명과학부 학부생들은 연구를 직접 보고 배우는 현장 경험을 쌓기 위해 대부분 교내 연구실에서 인턴 활동을 한다. 작년에는 코로나19의 영향으로 이러한 활동이 전반적으로 주춤했다. 하지만 언제가 될지 모르는 팬데믹 종식까지 마냥 기다리고 있을 수는 없었다. 그렇게 작년 7월부터 김빛내리 기초과학연구원(IBS) RNA 연구단장(서울대 생명과학부 교수)이 이끄는 연구실에서 인턴을 시작하게 되었다.
팬데믹 상황에서의 연구실팬데믹 시기 연구실의 모습은 평상시와는 사뭇 달랐다. 일주일에 한번 있는 랩 미팅부터 국제 학회까지 모두 화상 또는 온라인으로 이뤄졌다. 물론 화면 속 사람과 의견을 나누는 일은 좀처럼 익숙해지지 않았다. 다만 직접 해외로 나가야 하는 기존의 대면 학회 보다 접근성이 높아졌다는 장점은 있었다. 학교 수업 또한 비대면으로 진행됐기에 대학원생과 인턴들이 모두 연구실에서 수업을 듣고 시험을 보는 진풍경이 펼쳐지기도 하였다. 사실 필자가 인턴을 신청할 때까지만 해도 RNA 연구단에서 발표한 사스코로나바이러스-2 관련 연구성과는 없었다. 그런데 얼마 후 유전체와 전사체 분석을 통해 사스코로나바이러스-2(SARS-CoV-2) 고해상도 유전자 지도를 완성한 논문이 발표되었다(Kim et al., 2020). 연구실에 들어가 보니 정기 랩 미팅 외에 바이러스 미팅이 따로 있을 만큼 연구가 활발히 이뤄지고 있었다. 많은 우수한 연구원들이 사스코로나바이러스-2 연구에 매진하는 것을 보며, 사태의 조속한 진정을 위해 과학계에서 얼마나 노력하고 있는지 실감하였다. 인턴 시작 직후 앞으로 참여할 프로젝트를 선택했다. 가능한 선택지는 두 가지였다. 하나는 RNA 연구단의 주력 분야인 마이크로RNA(miRNA)였고, 다른 하나는 막 연구가 시작된 사스코로나바이러스-2 관련 프로젝트였다. 후자의 경우 우리 연구실에서는 미개척 분야라는 점에서 고민이 되었지만 인류의 가장 긴박한 문제를 과학의 힘으로 해결하는 숭고한 작업에 참여하고 싶었고, 이때가 아니면 없을 기회라는 생각도 들었다. 그렇게 사스코로나바이러스-2 연구팀에서 인턴 활동을 하게 되었다.
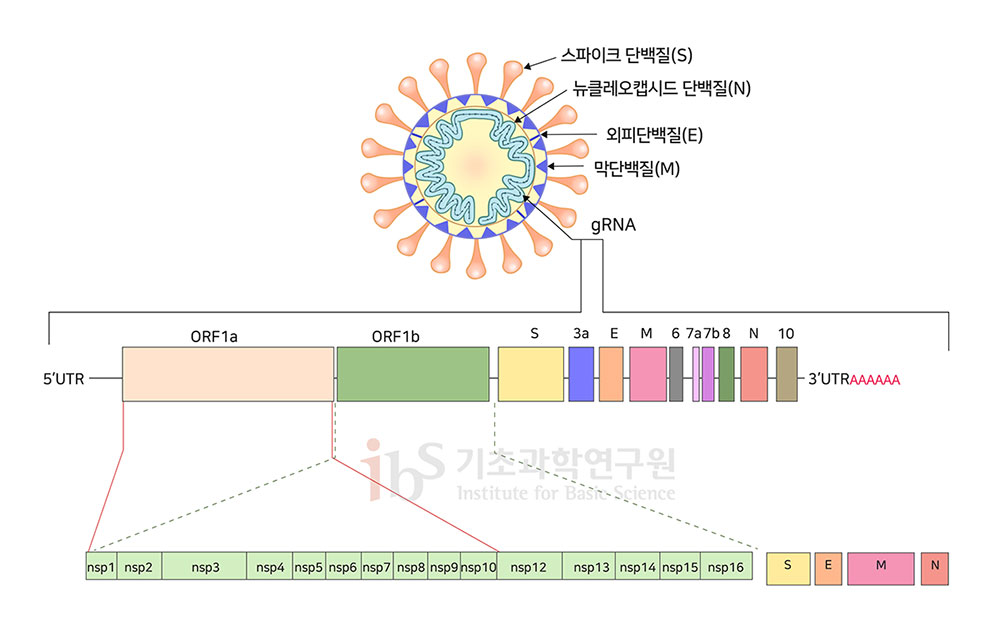
사스코로나바이러스-2 Nsp2의 기능을 찾아서사스코로나바이러스-2의 껍질 안에서는 gRNA(유전체RNA‧genomic RNA)라고 불리는 RNA가 바이러스의 유전 정보를 암호화한다. gRNA는 숙주세포로 들어가 분자 시스템에 의해 번역되어 27개의 바이러스 단백질을 만들어낸다. 이렇게 만들어진 단백질들은 각각 다른 기능을 수행하며 바이러스의 생존과 증식을 매개한다. 이중 16개의 비구조단백질(nsp)이 바이러스의 복제를 주도하는 것으로 알려져 있다(Astuti & Ysrafil, 2020). 필자가 참여하는 프로젝트에서는 다른 코로나바이러스 단백질들과 달리 현재까지도 그 기능에 대한 이해가 미진한 nsp2(nonstructural protein 2)에 초점을 맞춰 연구하고 있다. 특정 유전자나 단백질 기능 탐구에 가장 유용한 생물학적 방법은 기능을 없앤 변이체(knockout mutant)를 만든 후 그 변이에서 표현형을 관찰하는 것이다. 즉 nsp2의 기능을 알기 위해서는 이 단백질을 암호화하는 유전자를 없앤 바이러스의 특징을 정상 바이러스와 비교하면 된다. 이와 함께 특정 단백질과의 결합을 못하게 만든 변이, 특정 세포 내 구역으로 위치하지 못하게 만든 변이 등을 활용할 수도 있다. 유전체 변이 바이러스 제작에는 몇 가지 단계가 필요하다. 우선, 바이러스 유전체를 박테리아 플라스미드와 같이 조작하기 쉬운 전달체로 옮긴 후 유전자 삽입‧삭제‧치환 등 원하는 변이를 일으켜야 한다. 이렇게 만들어진 변이 유전체는 DNA 상태다. 사스코로나바이러스-2의 유전체는 RNA이므로, 세포 외 전사(in vitro transcription) 기술을 이용하여 DNA로부터 RNA 유전체를 만들어야 한다. 마지막으로 이러한 변이 RNA 유전체를 바이러스에 감염될 수 있는 숙주세포에 주입하면 RNA로부터 바이러스 단백질이 번역되고, 유전체가 복제되면서 변이 바이러스가 생산된다(Xie et al., 2020). 필자가 속한 연구팀은 이렇듯 nsp2 변이 바이러스를 이용해 nsp2 기능을 규명하고 바이러스를 이해하고자 노력 중이다.
팬데믹에 대처하는 과학자들의 자세살아있는 사스코로나바이러스-2를 다루는 실험은 모두 생물 안전 3등급(BSL3) 이상의 연구 시설에서 이루어져야 한다. 특별한 교육을 받은 연구자만 방호복을 입고 실험에 참여할 수 있다. 다행히 서울대 관악캠퍼스 인근의 국제백신연구소(IVI)와 협력하여 BSL3 시설을 이용할 수 있었다.
그런데 RNA 생물학 연구실은 원래 고위험 바이러스를 다루지 않았기 때문에, 사스코로나바이러스-2 연구 초창기만 해도 BSL3 실험이 가능한 연구자가 없었다. 따라서 질병관리본부 등과 협력하여 불활화 된 바이러스 샘플을 받아 실험을 진행했다. 하지만 이러한 방식으로는 연구에 한계가 있어 많은 연구원이 BSL3 실험에 자원하였고, 현재 직접 BSL3 실험을 진행하고 있다. 위험에 노출될 수도 있는 실험에 선뜻 나서는 연구실 선배들에게 존경심이 들었다. 우리 연구실뿐만 아니라 전 세계의 많은 연구진이 이렇게 적극적으로 사스코로나바이러스-2 연구에 나서고 있기에 인류는 갑자기 출현한 신종 바이러스의 이해에 빠르게 접근할 수 있었다. 원래 바이러스를 다루지 않던 연구진들도 각자가 가진 강점을 최대한 발휘하면서 바이러스의 비밀을 풀고 팬데믹 사태 진정을 위해 노력하고 있다. 1년만에 이뤄낸 백신 개발이라는 성과는 이러한 노력의 산물 중 하나다. 이례적으로 빨랐던 속도뿐만 아니라 최초의 mRNA 백신을 개발했다는 점도 의의가 크다. 이번 백신 개발은 사스코로나바이러스-2 팬데믹을 종식시킬 무기를 얻었다는 성과 그 자체로도 중요하지만, 앞으로 다른 바이러스의 위협이 도래하더라도 신속하고 효과적으로 대처할 수 있는 기술을 확립했다는 점에서 더욱 고무적이다. 게다가 백신의 개발은 RNA 합성 및 전달 기술 등 수많은 부수 기술들의 발전을 동반한다. mRNA를 통한 유전자 치료 등 많은 분야의 발전이 기대되는 이유다. 글을 마치며생명과학 전공 학부생으로서 팬데믹 시기 사스코로나바이러스-2 연구의 최전선에 참여할 수 있었던 것은 큰 영광이었다. 기초과학이 우리 일상 생활과 얼마나 밀접한 연관이 있는가를 이번에 새롭게 느낄 수 있었다. 한편으로는 그런 가치 있는 연구가 이루어지고 있는 곳에서 연구에 참여하고 있다는 생각에 자부심이 생기기도 하였다. 밤을 새워가며 석학들의 발표를 들은 것도 소중한 경험이었다. 시차 때문에 온라인 학회를 새벽에 참여해야 했지만, 피곤함도 잊은 채 세계의 과학자들이 인류 문제 해결을 위해 지성을 나누는 자리를 흥미진진하게 지켜보았다. 이렇게 얻은 경험과 감동을 든든한 자양분 삼아 향후 과학 발전과 인류 문제 해결에 기여할 수 있는 생명과학 연구자로 성장하고자 노력할 것이다. 이러한 배움의 기회를 주신 김빛내리 단장님과 연구실 분들께 감사를 전하며 글을 마친다. ▣ 참고문헌Kim et al. (2020). The Architecture of SARS-CoV-2 Transcriptome. Cell 181, 914-921. Rastogi, M., Pandey, N., Shukla, A. et al. SARS coronavirus 2: from genome to infectome. Respir Res 21, 318 (2020). https://doi.org/10.1186/s12931-020-01581-z Xie et al. (2020). An Infectious cDNA Clone of SARS-CoV-2. Cell Host & Microbe 27, 841-848. Astuti, I., & Ysrafil (2020). Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2): An overview of viral structure and host response. Diabetes & metabolic syndrome 14, 407–412. 글 | 이성한 서울대학교 생명과학부 4학년 편집 | IBS 커뮤니케이션팀 발행일 | 2021년 5월 12일 본 글의 저작권은 기초과학연구원에 있습니다. 무단 전재를 금지하며 공유‧인용 및 재사용 시에는 출처를 명시해주시기 바랍니다. |
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 박정훈 042-878-8217
- 최종수정일 2023-11-28 14:20