 뉴스센터
뉴스센터
인류의 강력한 적, 바이러스의 생존 전략바이러스와의 전쟁이 끝나지 않고 있다. 인류는 긴 역사동안 바이러스와 싸워왔다. 바이러스는 숙주세포의 면역 시스템을 피하기 위해 저마다의 생존 전략을 세운다. 지피지기면 백전백승. 바이러스의 생존 전략을 알아야 바이러스를 공격할 과학적 전략도 찾아낼 수 있다. [함께 읽으면 좋은 기사]
B형간염바이러스의 생존전략: 숙주세포를 역이용최근 기초과학연구원(IBS) RNA 연구단은 B형간염바이러스(HBV)와 거대세포바이러스(CMV)가 스스로 생존하는 전략을 규명했다. 김빛내리 단장이 이끄는 연구팀은 이들 바이러스가 숙주세포의 RNA 보호시스템을 역이용해 생존함을 규명했다. HBV와 CMV는 뚜렷한 치료법이 없었다. 바이러스가 자신을 보호하는 원리와 메커니즘이 밝혀지지 않았기 때문이다. RNA 연구단은 RNA 안정성에 중요한 역할을 하는 RNA 꼬리에서 실마리를 찾았다. 자체 개발한 RNA 염기서열 분석법인 ‘꼬리서열분석법(TAIL-seq)’을 적용한 결과 HBV와 CMV의 RNA에 다양한 염기로 이뤄진 ‘혼합꼬리*’가 존재함을 발견했다.
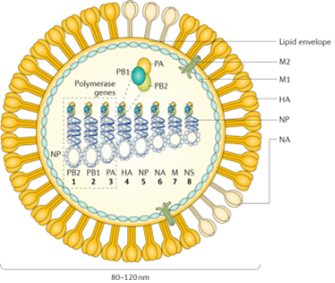
혼합꼬리는 원래 세포가 자신의 RNA를 보호하기 위해 활용하는 시스템이다. RNA 연구단은 2018년 혼합꼬리가 RNA의 분해를 막아 유전자를 활성화하는 데 기여한다는 사실을 밝힌 바 있다. 요컨대 일부 바이러스 역시 RNA 안정성을 높이고자 숙주세포의 자원을 활용하고 생존 전략을 모방하여 혼합꼬리를 만들어낸다는 것이다. 이 연구결과는 2020년 5월 국제학술지 ‘Nature Structural & Molecular Biology)’에 실렸다. 인플루엔자 바이러스의 생존전략 : 잦은 변이인플루엔자는 외피를 보유하고 있는 바이러스로 오르토믹소바이러스과(Orthomyxoviridae)에 속한다. 인플루엔자 바이러스는 8개(PB2, PB1, PA, HA, NP, NA, M, NS)의 분절된 단일가닥 음성 RNA 게놈(positive-sense single-stranded RNA)을 가지고 있다. 이 RNA가 숙주세포 안으로 침투하면 본격적인 증식활동이 펼쳐진다. 인플루엔자 바이러스의 아형(subtype)은 표면 당단백질인 혈구응집소(hemagglutinin‧HA)와 뉴라미니다아제(neuraminidase‧NA)에 의해 결정된다. 최근 박쥐로부터 H17N10과 H18N11 아형이 보고되어 현재는 18개의 HA 아형과 11개의 NA 아형이 있다. 인플루엔자 바이러스는 A, B, C, D의 네 가지 형으로 구분되고 사람, 조류, 야생동물 및 산업동물에 감염된다. 그중 A형과 B형이 사람에게 감염되어 독감을 유발하는 특징이 있다.
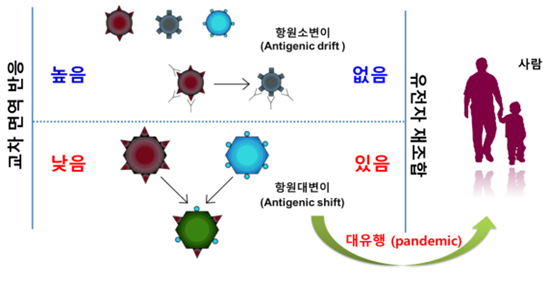
인플루엔자 바이러스는 유전자가 재조합되는 ‘항원 대변이(antigenic shift)’와 특정 유전자의 점 돌연변이에 의한 ‘항원 소변이(antigenic drift)’가 빈번하게 발생하며 신종 또는 변종 인플루엔자 바이러스가 등장하고 있다. 특히, 항원 대변이에 의한 변이 바이러스는 종의 장벽을 뛰어넘는 스필오버(spillover) 감염을 일으킬 수 있다. 면역력이 없는 숙주의 경우 폭발적인 감염이 일어나게 되므로 팬데믹으로 발전할 가능성이 크다.
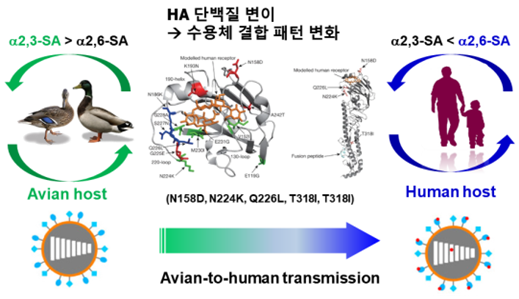
20세기만 해도 3번(1918~1919년 H1N1형 스페인독감, 1957~1958년 H2N2형 아시아독감, 1968~1969년 H3N2형 홍콩독감)의 인플루엔자가 유행했고, 21세기에는 2009년 H1N1형 신종 인플루엔자 바이러스 대유행이 발생했다. 대유행의 원인은 인플루엔자 바이러스의 항원 대변이에 의한 것으로 이전에 유행했던 인플루엔자의 감염이나 백신에 의해 형성됐던 체액성 면역반응이 바이러스 변이로 인해 방어 기능을 하지 못했기 때문인 것으로 밝혀졌다. 인플루엔자 바이러스의 HA 당단백질은 숙주세포 표면의 시알산(sialic acid)과 결합하고 세포에 침투하는 역할을 하고 있어 백신의 타깃으로 활용된다. 일반적으로 조류인플루엔자와 사람 또는 돼지 인플루엔자 바이러스의 HA 당단백질은 숙주세포와 결합하는 수용체 결합 선호도(receptor-binding preference) 때문에 자연 방어가 유지되지만, HA 당단백질은 항원 소변이가 빈번하게 발생되어 종간 감염을 유도한다. 2013년에 중국에서 발생되었던 인체감염 H7N9 인플루엔자 바이러스의 경우가 좋은 예라 할 수 있다. 야생조류와 가금류(닭, 오리 등)에서 유행하던 낮은 병원성의 H7형 조류인플루엔자 바이러스가 지속적인 조류와의 접촉으로 다양하게 진화하였고 특히 HA 당단백질이 사람의 숙주세포에 감염될 수 있도록 변이되었다(Lancet. 2013;381:1926-32). 변이된 바이러스에 감염된 조류와 사람이 접촉하여 변이 바이러스가 사람에게 감염되었고 이로 인하여 많은 사망자가 발생하였다. Yoshihiro Kawaoka 교수는 HA 당단백질의 변이가 인플루엔자 바이러스의 특성 변화에 중요한 요소임을 실험적으로 증명하였는데, H5N1 조류인플루엔자 HA 당단백질에 사람에게 감염되는 H1N1 인플루엔자 바이러스 HA 당단백질의 일부 아미노산 염기서열 (N158D, N224K, Q226L, T318I, T318I)을 인위적으로 치환시켰을 경우 H5N1 조류인플루엔자가 사람에게 병원성과 전파성이 증가하는 바이러스로 변이될 수 있음을 실험적으로 증명하였다(Nature 2012;486:420–428).
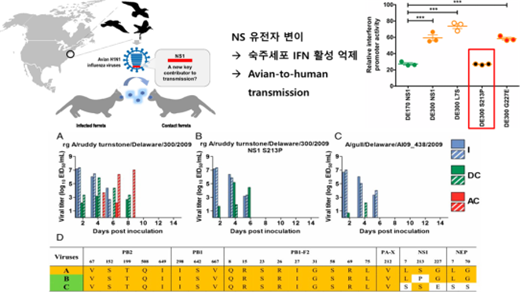
바이러스의 비구조단백질(non-structure protein, NS)은 숙주세포의 면역 활성을 억제하는 기능이 보고되었다. 인플루엔자 바이러스의 NS 유전자는 NS1과 NEP(nuclear export protein) 두 가지 단백질에 대한 유전정보를 가지고 있는데, NS1 단백질은 숙주세포의 인터페론 mRNA의 처리 과정을 억제하여 바이러스가 숙주의 선천성 면역기전으로부터 회피하게 하는 역할을 한다. 지난 2017년 Mark Zanin 교수는 야생조류에서 유행하고 있는 조류인플루엔자 바이러스가 다양하게 변이되고 있음을 확인하였고 특히 NS 유전자 변이가 변이된 조류인플루엔자 바이러스가 사람 숙주세포의 인터페론 활성을 억제하여 사람에게 공기 전파(airbone transmission) 가능성이 있음을 인플루엔자 바이러스 대표적인 인체감염 모델 동물인 페럿을 통해 증명하였다(PNAS. 2017;114(42):11217-11222).
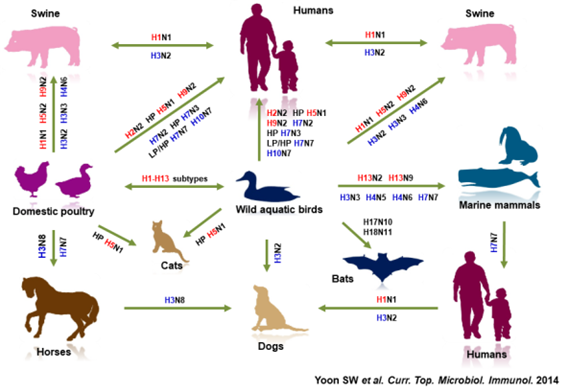
인플루엔자 바이러스는 대표적인 인수공통감염병 바이러스로 지속적인 변이 전략으로 다양한 숙주에 감염될 수 있는 형태로 진화하고 있다. 항원 대변이가 발생하면 새로운 재조합 바이러스에 대한 면역력이 형성되어 있지 않기 때문에 바이러스가 빠르게 전파되고 감염률이 증가되며 증상이 심각해지는 경우가 많다.
인플루엔자 바이러스의 종간전파를 방지하기 위해서는 사람과 야생동물과의 접점(interface)을 줄이는 것이 매우 중요하며 자연 숙주(조류 및 가금류, 야생동물 등)와 인간 사이의 인플루엔자 바이러스에 대한 지속적인 감시와 야생동물과 인간의 직접적인 접촉을 줄이거나 없애는 것이 향후 새로운 인수공통 바이러스 출현을 예방하는 데 매우 중요할 것이다. 본 콘텐츠는 IBS 공식 블로그에 게재되며, https://blog.naver.com 에서 확인하실 수 있습니다. |
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 임지엽 042-878-8173
- 최종수정일 2023-11-28 14:20