 뉴스센터
뉴스센터
RNA와 단백질의 결합자리, 염기 종류에 따라 정확히 찾아낸다- 유전자 발현에 중요한 RNA-단백질 간 결합 원리 규명 기대 - 기초과학연구원 RNA 연구단 김종서 연구위원(서울대 조교수)·김빛내리 단장(서울대 석좌교수)은 세포 내 단백질에서 RNA와 결합을 형성하는 ‘RNA 결합자리1)’를 염기 종류에 따라 정확하게 찾아내는 기법을 개발했다. 생명현상 조절에 필수적인 RNA-단백질 상호작용의 원리 규명에 크게 기여할 것으로 기대된다.
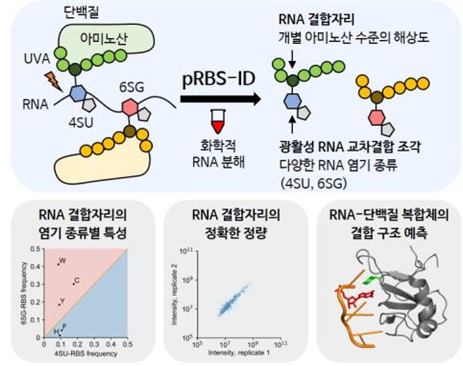
RNA 결합자리의 동정은 세포 기능 조절을 규명하기 위한 핵심 단계라고 할 수 있다. RNA에 단백질이 결합하여 번역 효율, 안정성, 세포 내 위치 등 단백질 생산과정을 조절해 정상적인 유전자를 발현시키기 때문이다. 이때 RNA 결합자리를 확인하려면 작은 단백질 조각의 질량을 측정해, 해당 조각의 아미노산 및 단백질 내 위치를 추론하는 ‘질량분석2)’ 방법이 필요하다. 연구진은 지난해 짧은 파장의 자외선(UVC)3)과 불산을 적용, RNA 내 유라실4)과 단백질의 교차결합을 형성하여 RNA 결합자리를 찾는 기술을 개발했다. 그런데 이 기술로는 RNA-단백질 상호작용의 복합적 파악이 어려웠다. RNA-단백질 교차결합 형성 효율이 매우 낮으며, 가능한 RNA 염기 종류도 유라실 하나뿐이었기 때문이다. 연구진은 긴 파장의 자외선(UVA)5)과 광활성 RNA6) 표지법을 활용해 작년 연구의 한계를 극복했다. 우선 세포 내 RNA를 4-티오유리딘과 6-티오구아노신7) 두 종류의 광활성 염기로 표지했다. 이후 UVA를 이용해 결합된 단백질과 특이적 교차결합을 유도하고, 단백질에 결합된 긴 RNA를 불산 처리하여 화학적으로 가수 분해했다. 그리고 질량분석 방법으로 남은 RNA 조각의 분자량을 확인했다. 이 정보를 토대로 4-티오유리딘과 6-티오구아노신의 각 염기 종류에 해당하는 특이적 RNA 결합자리를 고효율로 동정해냈다. 또한, 데이터 분석 프로그램을 발전시켜 RNA 결합자리를 포함하는 펩타이드를 정확히 정량했다.
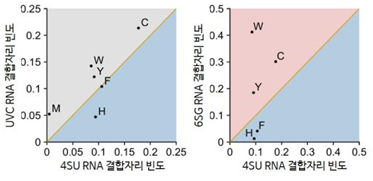
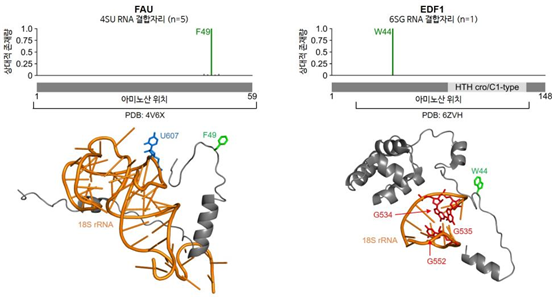
이로써 연구진은 염기 종류 및 교차결합 방식에 따른 RNA-단백질 상호작용 양상의 차이를 면밀히 규명했다. 이는 새로 발견한 광활성 RNA 결합자리 뿐 아니라, 기존 UVC를 이용한 RNA 결합자리까지 망라하는 성과다. 나아가 RNA-단백질 복합체 구조 데이터를 접목해, 질량분석으로 규명한 RNA 결합자리가 밝혀진 단백질-RNA 구조와 일치하는 염기 종류와 상호작용함을 확인했다. 또 단백질의 구조가 불안정하여 기존 데이터로 파악할 수 없었던 RNA-단백질 상호작용도 RNA 결합자리를 통해 밝혀냈다. 이번에 개발한 질량분석 기법과 새로 동정한 3,000개 이상의 RNA 결합자리 정보는 RNA-단백질 상호작용에 의한 생명현상 조절 이해에 활용될 수 있어 가치가 크다. 특히 광활성 RNA의 대사표지와 최근 획기적으로 개선된 단백질 구조 예측 프로그램8)들을 접목하면, RNA-단백질 상호작용의 동적 변화와 분자적 기전을 세밀히 이해할 수 있으리라 기대된다.
이번 연구성과는 Nature Communucations(IF 14.92)에 10월 15일 온라인 게재됐다. IBS 커뮤니케이션팀 1) RNA 결합자리 (RNA-binding site): RNA 결합단백질에서 RNA를 직접 인지하여 결합하는 아미노산 자리. 2) 질량분석 (Mass spectrometry): 전체 분자 및 이를 쪼갠 분자 질량을 각각 측정해 분자의 구성을 밝히는 기술. 3) UVC: RNA 결합단백질에서 RNA를 직접 인지하여 결합하는 아미노산 자리. 4) 유라실 (Uracil): RNA를 이루는 네 가지 염기(아데닌, 구아닌, 사이토신, 유라실) 중 하나. 5) UVA: 광활성 RNA-단백질 교차결합을 형성할 수 있는 비교적 긴 파장(365 nm)의 자외선. 6) 광활성 RNA (Photoactivatable ribonucleosides): 염기 내 산소 원자 하나가 황 원자로 치환되어, 특정 파장의 자외선에 의해 활성화되어 단백질과 교차결합을 형성하는 RNA. 4-티오유리딘과 6-티오구아노신이 있다. 7) 4-티오유리딘, 6-티오구아노신: 광활성 RNA의 종류로, 각각 유리딘 및 구아노신과 대응됨. 8) 2021년 7월 발표된 AlphaFold(Google Deepmind)와 RoseTTAFold(David Baker lab)가 있다. |
|||
|
|
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 나희정 042-878-8155
- 최종수정일 2023-11-28 14:20