 뉴스센터
뉴스센터
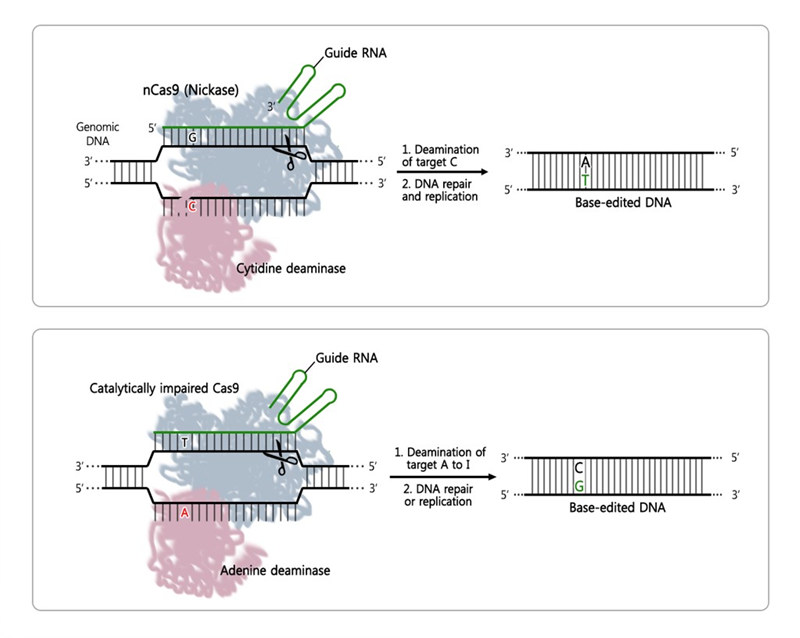
아데닌 염기만 바꾸는 염기교정 가위 정확성 밝혀절단 유전체 시퀀싱 기법 변형해 확인한 결과, 인간 유전체 32억 개 중 평균 60곳만 변이 생명체에 관한 모든 정보를 담고 있는 DNA는 네 개의 염기가 서로 쌍을 이뤄 나열된 구조다. 아데닌(A)은 티민(T)과 짝꿍이고, 시토신(C)은 구아닌(G)과 짝을 이룬다. 염기쌍이 중요한 이유는 DNA의 구조와 조합을 이루는 기본 단위이자 염기 하나만 잘못되어도 유전질환이나 질병이 발생할 수 있기 때문이다. DNA 두 가닥을 모두 자르는 기존 3세대 유전자가위인 크리스퍼 Cas9 혹은 Cpf1과 달리 단일 염기 하나만 바꾸는 기술에 과학계는 단일 염기 하나만을 바꿀 수 있는 인공제한 효소가 등장하자 큰 기대에 부풀었다. 2017년 학계에 보고된 아데닌 염기교정 유전자가위(Adenine Base Editor, 이하 아데닌 염기교정 가위)는 아데닌(A)을 구아닌(G)으로 바꿀 수 있다. 난치성 유전질환 연구와 치료에 진전을 가져올 도구로 주목을 받고 있지만 유전자 교정기법으로 널리 활용되려면 선행되어야 하는 연구가 있다. 바로 아데닌 염기교정 가위의 정확성을 밝혀야만 한다. 우리원 유전체 교정 연구단은 그간의 정확성 연구에 대한 노하우를 바탕으로 아데닌 염기교정 가위의 정확성을 밝히는데 성공했다. 연구진은 인간 유전체 32억 개 중 평균 60곳에만 변이를 일으킨다는 사실을 국제학술지 네이처 바이오테크놀로지(Nature Biotechnology)에 논문을 게재했다.
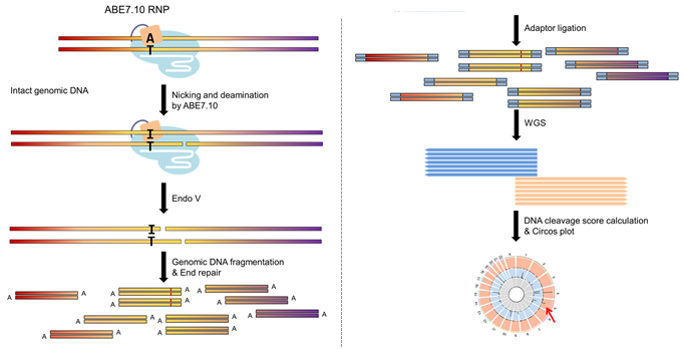
IBS 연구진은 아데닌 염기교정 가위의 정확성을 확인하고자 절단 유전체 시퀀싱(Digenome-seq) 기법을 변형하여 분석에 돌입했다. 절단 유전체 시퀀싱 기법은 그간 크리스퍼 Cas9, 크리스퍼 Cpf1 등 새로운 유전자가위의 정확성을 분석한 연구단의 기술력이 집약된 프로그램이다. 쉽게 말해 유전자가위를 처리한 뒤, 처리 전과 후를 비교하는 방식이다. 이번 연구에서는 두 가닥 절단이 아닌 한 가닥만 자르는 유전자 교정 기법의 정확성을 파악해야 하기에 특정 효소(Endo V, 이노신 특이적 절단 시약)를 추가했다. 실험 결과, 아데닌 염기교정 가위는 인간 유전체 32억 개 중 평균 60곳에만 변이를 일으키는 것을 확인했다.
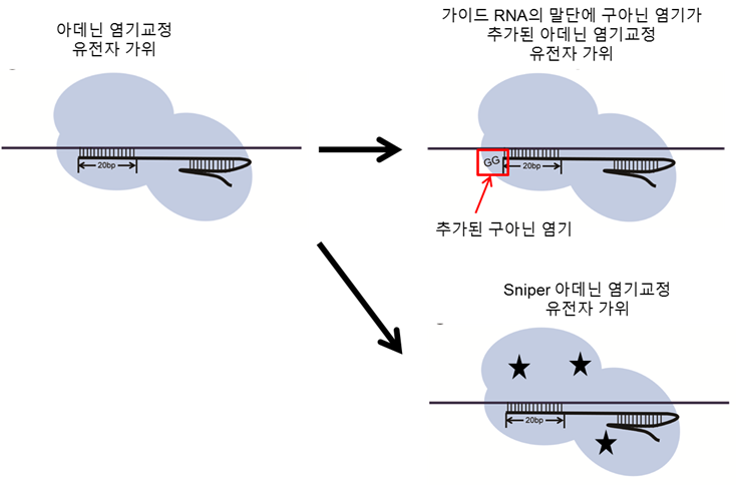
더 나아가 연구진은 아데닌 염기교정 가위의 정확성을 높이는 다양한 방법들을 제시했다. 첫 번재는 가이드 RNA 말단에 구아닌 염기를 추가하는 방법이다. 교정할 염기를 찾아가는 가이드RNA 끝에 구아닌 염기를 붙여 길이를 조절하면, 표적위치에서 작동 효율을 높이고, 오작동할 확률을 낮출 수 있다. 정확성이 높다고 알려진 유전자가위로 아데닌 염기교정 가위를 만드는 방법도 있다. 일명 저격수 유전자가위인 Sniper 유전자가위는 기존 크리스퍼 유전자가위보다 정확성이 높다고 알려져 있다. 전달방식의 변화도 고려할 수 있다. 아데닌 염기교정 가위를 DNA(Plasmid DNA)에 싣지 않고 탈아미노효소와 가이드RNA를 혼합한 형태로 세포에 직접 전달하면 정확도를 향상시켜 표적위치만 자를 수 있다. 연구진은 "염기교정 가위의 정확성이 입증된 만큼 앞으로 이를 활용해 단일 염기 변이를 유도하거나 교정해야 하는 유전자 및 줄기세포 치료제 개발, 고부가가치 농축산물 품종 개량 등에 널리 활용될 것으로 기대된다"고 말했다. IBS 유전체 교정 연구단은 2018년 4월 아데닌 염기교정 유전자가위로 동물의 특정 유전자 염기를 바꾸는데 최초로 성공해 같은 학술지에 연구성과를 게재한 바 있다. 2015년 자체 개발한 분석법(Digenome-seq)을 통해 3세대 유전자가위인 크리스퍼 Cas9과 크리스퍼 Cpf1은 물론 시토신(C)을 티민(T)으로 바꾸는 시토신 염기교정 가위의 정확성도 규명해 학계에 보고한 바 있다.
IBS 커뮤니케이션팀 |
|||
Center for Genome Engineering (유전체 교정 연구단)Publication Repository |
|||
|
|
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 한정민 042-878-8153
- 최종수정일 2023-11-28 14:20