 뉴스센터
뉴스센터
| 제목 | DNA 내부 이상 구조 제어법 발견…암 억제 활용 기대 | ||
|---|---|---|---|
| 보도일 | 2020-07-02 09:38 | 조회 | 2212 |
| 연구단명 |
유전체 항상성 연구단 |
||
| 보도자료 |
![hwp 파일명 : 200702_[IBS 보도자료]_DNA 내부 이상 구조 제어법 발견_암 억제 활용 기대(유전체 항상성_ NAR).hwp](/images/mimetype/hwp.gif) 200702_[IBS 보도자료]_DNA 내부 이상 구조 제어법 발견_암 억제 활용 기대(유전체 항상성_ NAR).hwp
200702_[IBS 보도자료]_DNA 내부 이상 구조 제어법 발견_암 억제 활용 기대(유전체 항상성_ NAR).hwp
|
||
| 첨부 |
![zip 파일명 : 200702_[IBS 보도자료]_그림 및 사진.zip](/images/mimetype/zip.gif) 200702_[IBS 보도자료]_그림 및 사진.zip
200702_[IBS 보도자료]_그림 및 사진.zip
|
||
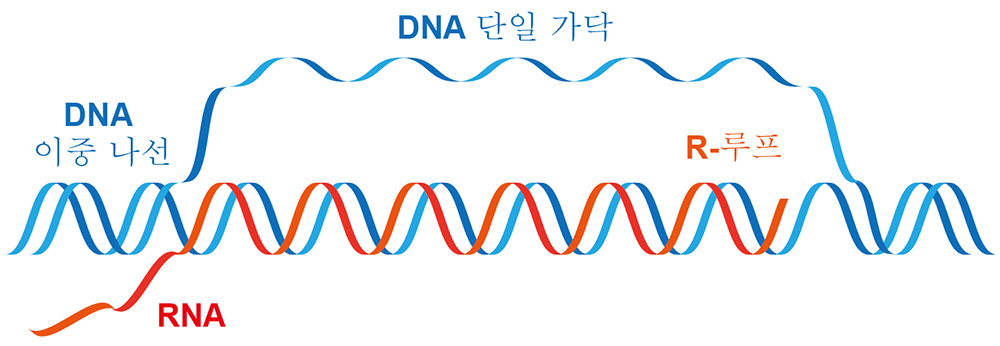
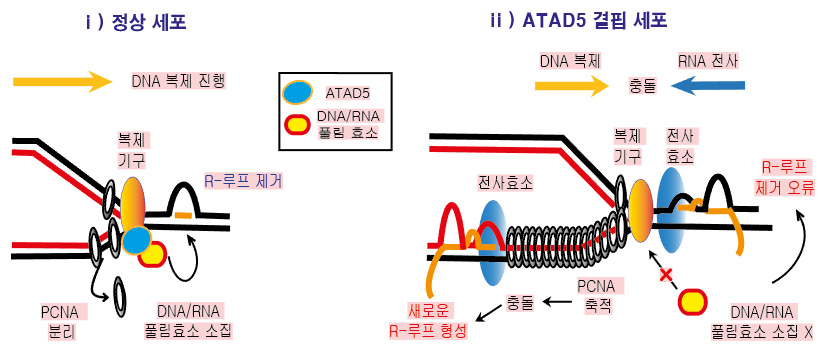
DNA 내부 이상 구조 제어법 발견…암 억제 활용 기대- 암 억제 단백질 ATAD5의 유전체 안정성 유지 원리 규명 - 세포가 DNA 내부의 이상 구조를 제어하는 방법이 밝혀졌다. 기초과학연구원(IBS, 원장 노도영) 유전체 항상성 연구단(단장 명경재) 이규영 연구위원팀은 암 억제 단백질 ATAD51)가 DNA 내 이상 구조 형성과 해소를 조절하여 유전체 안정성을 유지하는 원리를 규명했다. 우리 몸의 세포는 생명 유지를 위해 DNA 복제·전사·복구 등 다양한 대사 활동을 한다. 이때 RNA가 DNA 이중나선의 한 가닥에 결합한 ‘R-루프(R-loop)2)’가 일시적으로 형성되어 대사 과정 일부를 도운 후 해소된다. R-루프가 해소되지 않고 장시간 유지되면, RNA 전사 단백질이 DNA 복제 단백질과 충돌하는 ‘전사-복제 충돌’이 일어난다. 이 경우 DNA 복제와 전사가 완료되지 못한 채 멈춰버린다. 이 상태에서 세포분열이 진행되면 DNA가 손상되어 유전정보 안정성이 떨어지고 암으로 이어질 수 있다. 유전체 항상성 연구단은 이전 연구에서 ATAD5 단백질이 DNA 복제 스트레스3)를 해소하여 안정적인 DNA 복제를 돕고 암 억제에 기여한다는 것을 밝혔다. 이번 연구에서는 ATAD5 단백질이 DNA 복제 과정에서 R-루프 형성을 제어하여 전사-복제 충돌을 해결함으로써 유전체 안정성을 유지하는 방법을 규명했다. 연구진은 우선 ATAD5 단백질이 R-루프 형성에 미치는 영향을 이해하기위해 siRNA4)를 이용하여 인간 세포 내 ATAD5 단백질 양을 줄였다. 그 결과 DNA 복제가 진행 중인 세포에서만 R-루프의 양이 증가했다. ATAD5 단백질이 R-루프 형성 억제에 핵심 요소라는 의미다. 또한 염색체 복제를 도와주는 PCNA5) 단백질이 과다 축적되어 RNA 전사 단백질과 전사-복제 충돌을 일으키고 새로운 R-루프가 형성되었다. 이를 통해 ATAD5 단백질이 DNA 복제 부위에서 PCNA 단백질을 분리하여 새로운 R-루프 형성을 미리 차단한다는 것을 알 수 있다. 추가적으로 연구진은 면역정제-질량분석법6)을 이용해 ATAD5 단백질이 R-루프를 풀어주는 DNA-RNA 풀림효소 단백질들과 상호작용함을 확인했다. ATAD5 단백질이 결핍되면 이 작용이 저해되어 DNA 복제 부위의 DNA-RNA 풀림효소 양이 줄어들었다. ATAD5 단백질이 DNA-RNA 풀림효소 양을 유지하여 복제 중인 DNA에 존재하는 R-루프를 제거한다는 의미다. 이규영 연구위원은 “이번 연구로 ATAD5 단백질이 DNA 복제 조절, DNA 복제 스트레스 해소뿐 아니라 DNA 내 이상 구조 제어 기능을 갖는다는 새로운 사실을 밝혔다”며 “R-루프는 암 발생과 밀접한 관련이 있는 DNA 복구, 노화와 관련된 텔로미어(Telomere) 길이 조절에도 중요하기 때문에 향후 암 치료제, 노화 억제제 개발에 기여할 것으로 기대된다”고 전했다. 이번 연구성과는 국제 학술지 핵산 연구(Nucleic Acids Research, IF 11.501)온라인 판에 6월 15일 게재되었다. 그림설명
1) ATAD5(ATPase family AAA domain-containing protein 5) 단백질 : ATAD5 단백질은 4개의 단백질(RFC2,3,4,5)과 복합체를 형성하여 PCNA를 조절하는 복제 조절 단백질이다. 2) R-루프(R-loop) : 전사 과정에서 만들어진 RNA가 DNA 이중 나선의 한 가닥과 결합하고, 나머지 한 가닥은 단일 나선 형태로 존재하는 DNA-RNA 혼성구조 3) DNA 복제 스트레스(DNA replication stress) : DNA 복제에 필요한 물질이 충분히 공급되지 않거나 세포가 유해물질에 노출되었을 때 DNA 복제가 멈추는 것. 복제 스트레스가 적절히 해소되지 못하면 유전정보 안정성이 떨어지고 암 발생으로 이어질 수 있다. 4) siRNA(small interfering RNA) : 특정 유전자 서열에 특이적인 siRNA를 세포에 발현시키면 RNA 간섭(RNA interference) 기작을 통해 특정 유전자의 전령 RNA(messenger RNA) 양을 줄여, 결과적으로 특정 단백질 양을 줄일 수 있다. 5) PCNA(Proliferating Cell Nuclear Antigen, 증식성세포핵항원) : DNA에 결합하여 염색체 복제를 도와주는 단백질. 염색체 복제 과정에서 여러 단백질을 끌어와 복제를 돕고, 복제가 끝난 뒤 DNA와 분리된다. 6) 면역정제-질량분석법(Immunopurification-Mass spectrometry) : 특정 단백질에 특이적으로 결합하는 항체(단백질)를 사용하여 용액에서 해당 단백질 및 결합 단백질을 질량분석을 통해 확인하는 기술. |
|||
|
|
|||
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 나희정 042-878-8155
- 최종수정일 2023-11-28 14:20