IBS 연구성과
6월의 IBS 연구성과
1. 빛 쪼였더니 암세포가 번식하다가 스톱!
국내 연구진이 빛을 비추는 것만으로 암세포가 분열을 하지 못하도록 막는 데 성공했다.
허원도 기초과학연구원(IBS) 인지및사회성연구단 바이오이미징 그룹리더(KAIST 생명과학과 교수)는 빛을 비춰 작동하는 단백질 올가미를 이용해 세포 속 단백질을 억제하는 원천 기술을 개발하고 학술지 '네이처 메소드' 온라인판 5월 4일자에 발표했다.
연구팀은 빛으로 켜고 끌 수 있는 올가미를 만들기 위해 식물인 애기장대의 유전자를 이용했다. 애기장대의 특정 유전자는 청색광에 반응하는 단백질을 만들어내는데, 연구팀은 이 유전자가 만든 단백질을 이용해 청색광에 비춰졌을 때만 표적 단백질에 달라붙는 올가미(LARIAT)를 만들었다. 그 결과 빛을 비추면 수 초 만에 올가미가 형성돼 표적 단백질을 구속하고, 빛을 끄면 수 초에서 길게는 수 분 안에 올가미가 사라졌다.
연구팀은 인간 암세포에서도 올가미가 정상적으로 작동함을 보이기도 했다. 빛을 비추자 암세포 내에서 올가미가 형성되고, 올가미가 세포 분열에 이용되는 단백질을 차단해 암세포가 번식하지 못하게 된 것.
하지만 이번 연구결과가 항암치료로 응용되기 위해서는 넘어야할 산이 많다. 빛을 비추지 않으면 올가미가 사라지기 때문에 멈춰있던 암세포의 분열이 다시 재개된다. 허 교수는 "5분 마다 몇 초 씩 비춰주는 것만으로 계속해서 올가미를 유지할 수 있긴 하지만 치료제로 이용하려면 후속 연구가 더 필요하다"고 밝혔다.
이번 연구결과는 세포 내에서 특정 단백질이 어떤 위치에서 어떤 역할을 하는지 알아내는 데 활용될 전망이다. 빛을 세포의 국소부위에만 쪼이는 방법으로 세포 전역이 아닌 일부분에서만 단백질을 억제하는 것도 가능하기 때문이다. 허 교수는 축구를 예로 들어 "선수를 빼고 경기를 하면 그 선수의 역할을 알 수 있는 것과 같은 이치"라고 설명했다.
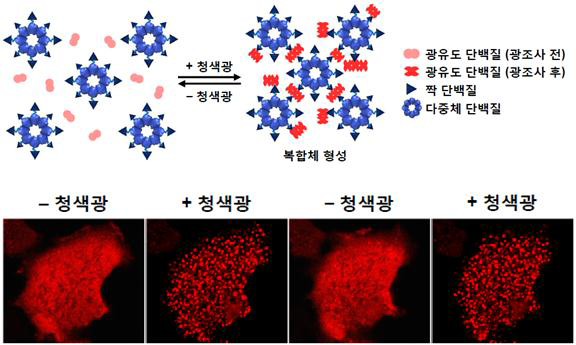
▲ 광유도 분자올가미 기술
2. 물에 녹는 친환경 금속 나노입자 개발
물속에서도 안정적으로 촉매 역할을 하는 친환경 금속 나노입자가 기초과학연구원 복잡계 자기조립 연구단의 김기문 단장(포스텍 교수) 연구팀에 의해 개발됐다.
100nm(1만분의1 밀리미터) 이하 크기의 금속 나노입자는 고유의 우수성으로 공업, 약학, 농업(비료) 분야에서 다양하게 활용되어 왔으나 톨루엔(toluene), 헥산(hexane)과 같은 유독성 액체를 용매로 사용하기 때문에 환경오염, 고비용, 중독 등을 유발하는 문제점을 안고 있었다.
하지만 연구팀은 이번 연구를 통해 유독성 용매가 아닌 물과 같은 환경 친화적인 용매에서 촉매활성을 가지면서 안정된 성질을 지니는 금속 나노입자-고분자 나노캡슐로 환경·안전·경제적 문제를 단번에 해결할 수 있는 가능성을 제시했다.
연구팀은 '쿠커비투릴'이라는 물질로 이뤄진 고분자 나노캡슐과 금속염을 이용하여 이런 문제를 해결한 것. 쿠커비투릴은 금속 나노입자를 뭉치지 않게 안정화 시키는 보호제 역할을 한다. 이렇게 개발된 금속 나노입자-나노캡슐은 물속에서 6개월 이상 안정된 상태를 유지해 안전성을 확보했고, 분산성, 촉매활성 등에도 높은 효과를 보였다. 또한, 여러 번 다시 사용할 수 있어 경제성도 뛰어났다.
이 성과는 5월 19일 화학 분야에서 최고의 권위지로 꼽히는 '안게반테 케미'(Angewandte chemie) 온라인판에 실렸다.
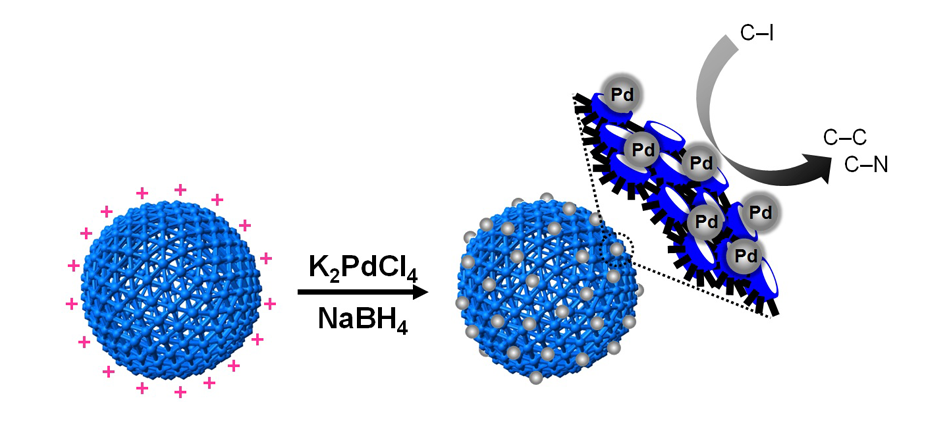
▲ 금속나노입자가 균질하게 도입된 고분자 나노캡슐
3. DNA 나노머신을 이용한 유전자 전달 및 항암 광열치료 규명
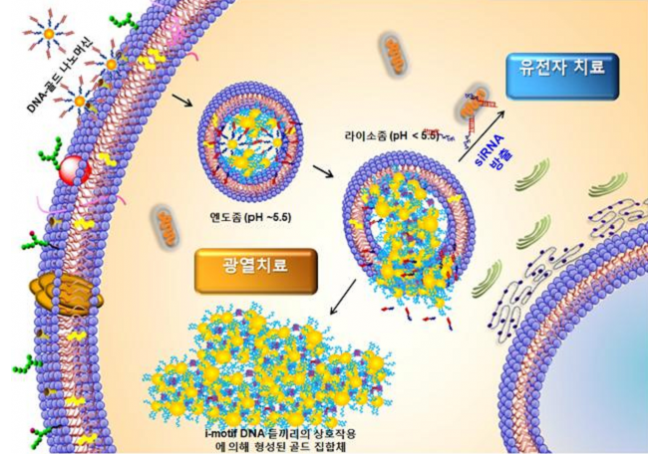
▲ i-motif DNA-골드 나노머신의 세포내부로 유입 후 작용 기작
국내 연구진이 항암치료를 극대화시킬 수 있는 신기술을 개발했다.
김원종 기초과학연구원(IBS) 복잡계 자기조립연구단 그룹리더 연구팀은 필요한 곳에만 지능적으로 유전자를 전달할 수 있는 DNA 나노머신을 개발하고 화학분야 권위지 'ACS 나노' 10일자 온라인판에 발표했다.
DNA 나노머신이란 생명체의 유전정보를 저장하는 DNA를 조립해 만든 나노미터 크기의 작은 구조체로, 산ㆍ염기 상태를 변화시키거나 빛과 온도를 조절해 움직임을 조종하는 것이 가능하다.
연구팀은 산도가 높은 환경이 되면 서로 모여 자기조립되는 DNA 나노머신을 디자인했다. 세포에 삼켜진 나노머신은 세포내 산성을 띠는 엔도좀(endosome)이란 공간으로 이동하게 되는데, 이곳의 산성 때문에 나노머신은 스스로 조립돼 한 곳에 뭉친 형태가 된다.
연구팀은 이 나노머신에 금 나노입자와 항암치료 유전자인 간섭RNA를 붙였다. 간섭RNA는 나노머신이 세포에 의해 삼켜질 때 1차적으로 세포에 전달돼 항암치료를 돕는다. 또한 자기조립 과정을 통해 한 곳에 뭉친 금 나노입자는 근적외선을 흡수할 수 있는 광학적 성질로 바뀌게 되어 근적외선을 이용한 광열치료 효과를 높일 수 있다.
손세진 연구원은 "광열치료를 병행하자 간섭RNA를 이용한 항암치료만 할 때보다 효과가 2.5배 높아졌다"며 "DNA 나노머신이 암세포만 특이적으로 골라 치료제를 전달하도록 만드는 것이 다음 연구과제"라고 설명했다.