 뉴스센터
뉴스센터
미토콘드리아 DNA 고친다…첫 동물실험 성공- 동물 미토콘드리아 DNA 교정 성공해 미토콘드리아 질환 치료에 돌파구 마련 -
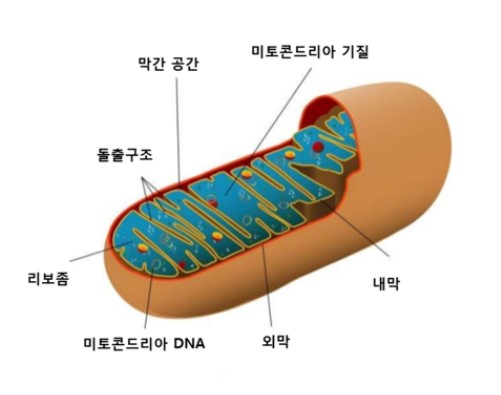
우리 몸 속 세포에는 에너지를 만들어내는 공장, ‘미토콘드리아(Mitochondria)’란 소기관이 있다. 미토콘드리아 DNA에 변이가 일어날 경우 시력·청력 뿐 아니라 특히 에너지가 많이 필요한 중추신경계·근육·심장 등에 치명적인 결함을 야기한다. 미토콘드리아 DNA는 모계 유전되기 때문에 어머니의 미토콘드리아 DNA에 결함이 있을 경우 다음 세대로 고스란히 전달된다. 미토콘드리아 질환은 5,000명 중 한 명 꼴로 발생하는 비교적 흔한 유전질환이지만 아직까지 마땅한 치료법이 없다. 현재 유전체 교정 기술로 널리 활용되는 크리스퍼 유전자가위(CRISPR-Cas9)는 미토콘드리아 DNA 교정이 불가하다는 한계가 있다. 크리스퍼는 자르고 싶은 목표 DNA 부위에 찾아가서 달라붙는 가이드 RNA이며, 캐스9가 이를 이용해 단백질을 잘라내는 가위 역할을 한다. 문제는 가이드 RNA가 미토콘드리아 막을 통과하지 못해 캐스9도 미토콘드리아 내부로 들어갈 수 없다는 점이다.
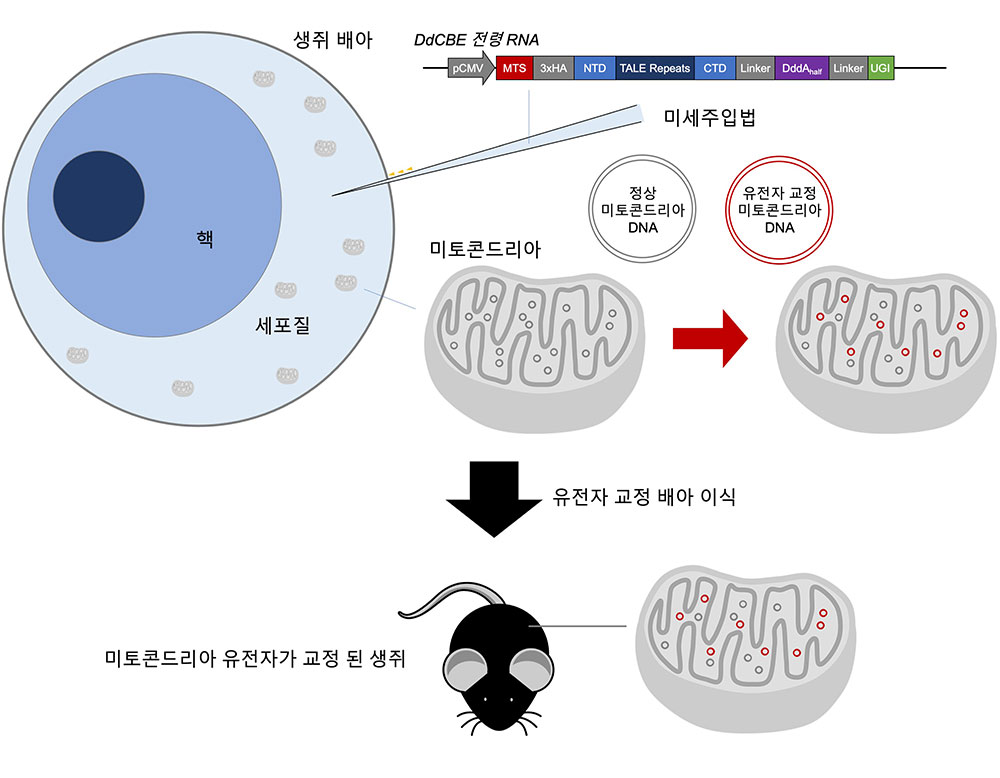
지난해 7월, 미국 브로드 연구소의 데이비드 리우(David Liu) 교수 연구진은 세균에서 유래한 DddA 탈아미노 효소를 활용하여 새로운 염기교정효소 ‘’를 제작함으로써 미토콘드리아 DNA 교정에 성공했다. 그러나 이는 세포 수준의 연구로, DdCBE가 동물 개체 수준에서도 정상 작동하는지 확인이 필요했다. 기초과학연구원(IBS, 원장 노도영) 유전체교정 연구단(단장 김진수)이 시토신 염기교정효소(DdCBE)1)를 이용해 생쥐 미토콘드리아 DNA의 특정 염기를 바꾸는데 성공했다. DdCBE를 동물에 적용한 세계 최초의 사례로서, 치료가 어려웠던 미토콘드리아 질환 연구와 치료제 개발에 기여할 것으로 기대된다. 연구진은 우선 다양한 조합의 DdCBE를 생쥐 세포주(생체 밖에서 계속적으로 배양이 가능한 세포 집합) 수준에서 선별하여 가장 효율이 높은 DdCBE를 선정하였다. 최적의 조건에서 DdCBE를 생쥐 배아에 미세주입하여 미토콘드리아 DNA에 작용시킴으로써 시토신 염기를 티민으로 치환하는 데 성공했다. 정확하고 효과적인 방식으로 미토콘드리아 DNA 서열이 변환된 동물을 최초 제작한 것이다.
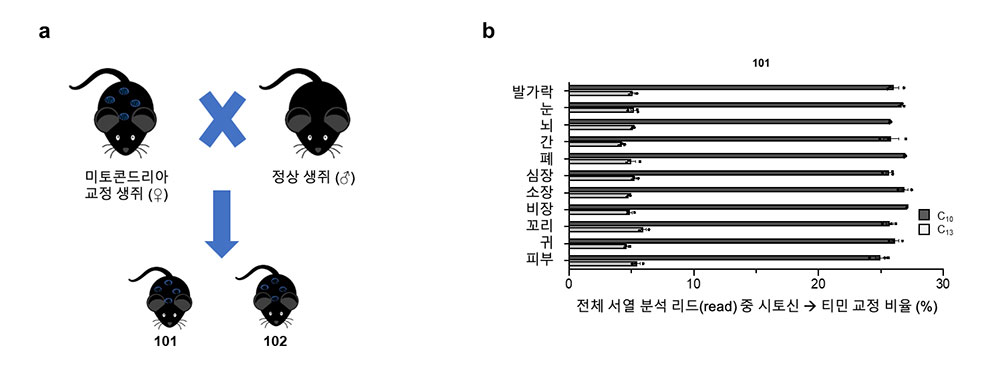
나아가 어미 생쥐의 교정된 미토콘드리아 DNA 서열이 다음 세대에게도 온전히 전달됨을 확인했다. DdCBE가 동물 개체 수준에서 정상 작동함을 최초로 확인한 것이다.
연구를 주도한 이현지, 이성현 선임연구원은 “미토콘드리아 DNA를 동물배아 수준에서 정밀하게 교정할 수 있게 됐다”며 “향후 미토콘드리아 질환 기작 연구와 치료제 개발에 새 길을 열 것으로 기대한다”고 전했다. 이번 연구결과는 오픈액세스 학술지인 네이쳐 커뮤니케이션즈 (Nature Communications, IF 11.878) 2월 19일 19시(한국시간) 온라인 판에 게재되었다. IBS 커뮤니케이션팀 1) DdCBE(DddA-derived cytosine base editor) : 세균의 독소에 유래된 DddA 탈아미노 효소를 두 조각으로 나누어 여기에 DNA에 염기 서열에 결합할 수 있는 TALE 단백질, 단백질을 미토콘드리아 내로 안내하는 서열(MTS : Mitochondrial Targeting Sequence), 우라실 글리코실레이즈 억제제(UGI : uracil glycosylase inhibitor)를 연결하여 만든 시토신 염기 교정 효소로, 2020년 7월 브로드 연구소 데이비드 리우 교수팀이 처음 학계에 보고하였다. |
|||
|
|
| 이전 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 임지엽 042-878-8173
- 최종수정일 2023-11-28 14:20