 뉴스센터
뉴스센터
| 제목 | 녹내장 발생 근본 원인 찾았다...새 치료법도 제시 | ||
|---|---|---|---|
| 보도일 | 2017-09-19 12:00 | 조회 | 8329 |
| 연구단명 |
혈관 연구단 |
||
| 보도자료 |
![hwp 파일명 : 170919_[보도자료]_녹내장 발생에 관여하는 신호전달체계 규명(혈관 연구단, JCI).hwp](/images/mimetype/hwp.gif) 170919_[보도자료]_녹내장 발생에 관여하는 신호전달체계 규명(혈관 연구단, JCI).hwp
170919_[보도자료]_녹내장 발생에 관여하는 신호전달체계 규명(혈관 연구단, JCI).hwp
|
||
| 첨부 |
 170919_그림 및 사진.zip
170919_그림 및 사진.zip
|
||
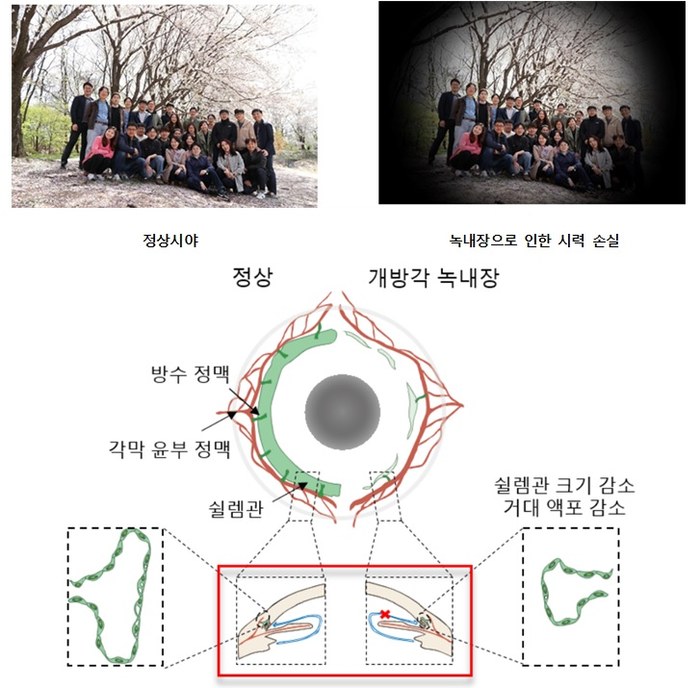
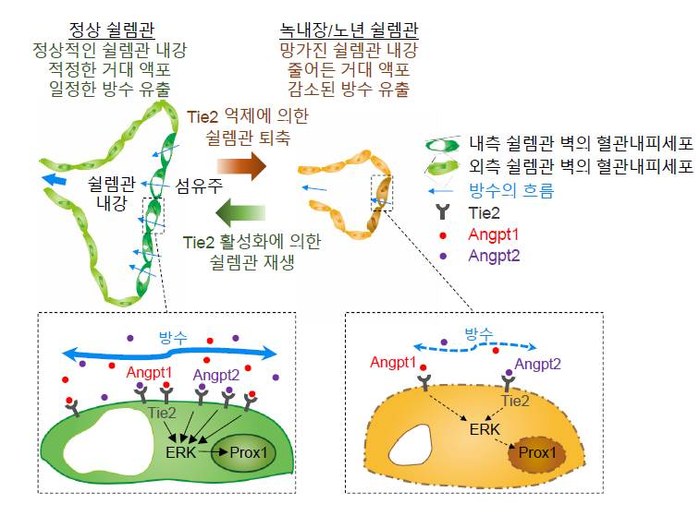
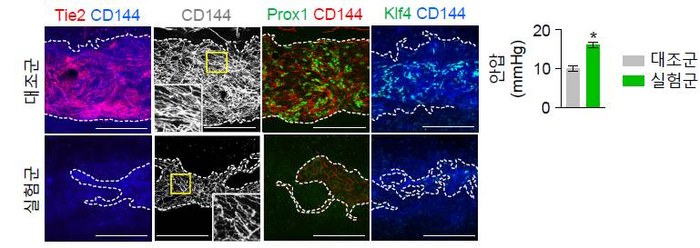
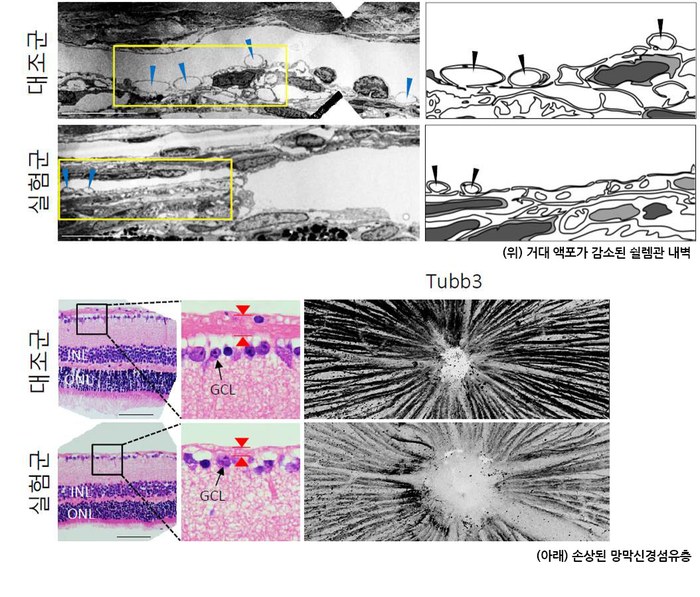
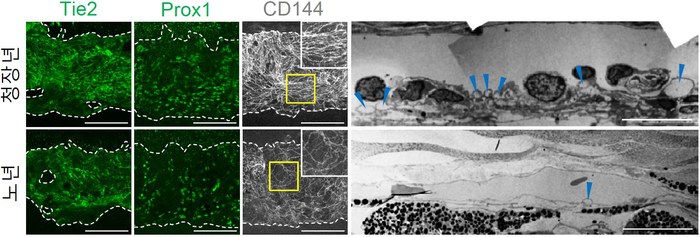
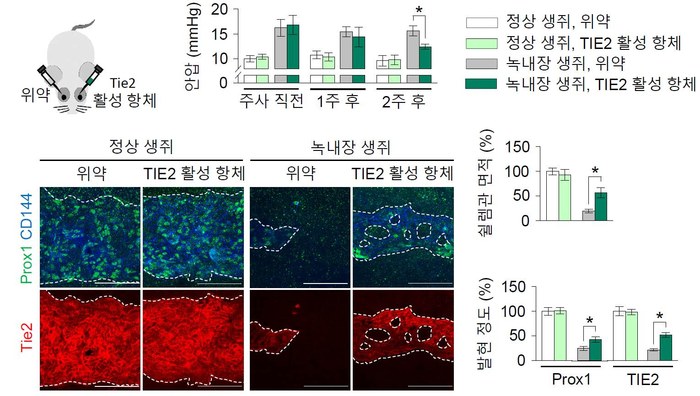
녹내장 발생 근본 원인 찾았다...새 치료법도 제시- 안압 조절하는 쉴렘관이 항상성 유지하는 원리 규명...항체 실험으로 안압 낮추는데 성공 - 기초과학연구원(IBS) 혈관 연구단 고규영 단장(KAIST 의과학대학원 특훈교수)과 김재령 연구원(KAIST 박사과정/안과전문의)이 녹내장(Glaucoma)이 발생하고 진행하는 근본적인 원인을 규명하고 새로운 치료방법을 제시했다. 녹내장은 안압이 상승해 시신경이 눌리거나 혈액 공급에 문제가 생겨 시신경이 망가지고 실명에 이르는 병이다. 증상이 나타날 땐 이미 시신경이 크게 손상된 상태라 완치가 어렵다. 전 세계 40세 이상 성인 인구의 3.5%가 녹내장을 앓고 있으며 국내에서도 환자가 빠르게 증가하는 추세다. 특히 전체 환자의 약 75% 이상을 차지하는 원발개방각녹내장의 경우 원인을 분자적 수준에서 밝히기 어려워 근본적인 치료법 마련에 한계가 있었다. 원발개방각녹내장 발병 기전의 이해를 넓힌 이번 연구로 그간 더뎠던 치료법 개발에 속도가 날 것으로 기대된다. 연구진은 안압이 안정적으로 유지되는 작동원리와 신호전달체계를 규명했다. 안압 조절에 중요한 기관인 쉴렘관1)의 항상성 유지를 Angiopoietin-TIE2 수용체 신호전달체계(이하 ANG-TIE2 신호전달체계)2)가 수행함을 밝혔다. 녹내장은 방수3)배출장치가 고장 나면서 발생한다. 눈 내부에서 생성된 방수는 섬유주를 지나 쉴렘관을 거쳐 혈관으로 배출된다. 안압은 방수가 생성되는 만큼 배출되어야 일정하게 유지되는데 방수배출장치에 문제가 생기면 안압이 상승한다. 원발개방각녹내장의 경우, 방수유출경로의 저항이 커지면서 방수가 제대로 빠져나가지 않아 발생하는 것으로 알려져 있으나 어떤 이유 때문에 저항이 커지는지는 알 수 없었다. 김재령 연구원과 박대영 연구원(박사후연구원/안과 전문의)은 혈관 성숙과 안정화에 필수적인 ANG 단백질과 TIE2 수용체가 각각 쉴렘관 주변부와 내피세포에 두드러지게 발현되는 것을 발견했다. 연구진은 ANG-TIE2 신호전달체계가 생후 초기 쉴렘관의 발달뿐만 아니라 성체가 된 이후에도 항상성 유지에 필수적일 것으로 예상했다. 실험 결과, 연구진은 쉴렘관 형성과 유지, 안압 조절에 있어 ANG-TIE2 신호전달체계가 핵심적인 역할을 수행함을 확인했다. ANG-TIE2 신호전달체계는 쉴렘관을 형성하고 내강을 유지해 방수 유출을 가능케 한다. 쉴렘관이 형성되는 동안에는 Prox1 전사인자4) 발현을 촉진하고 성체가 된 이후에는 적절한 양의 방수, 거대액포5), Prox1 전사인자 발현을 유지하여 쉴렘관의 항상성을 지킨다. 연구진은 녹내장이 유발된 상황에서 ANG-TIE2 신호전달체계의 활성화가 어떤 효과가 있는지 추가 실험을 진행했다. TIE2 수용체를 활성화하는 실험적 항체(ABTAA)가 쉴렘관의 내피세포에 작용하여 방수 유출을 증가시키고 안압을 낮출 수 있는지가 관건이었다. 쉴렘관이 망가져 안압 상승으로 녹내장이 유발된 실험군의 눈 속에 항체를 투여한 결과, 쉴렘관이 회복되면서 안압이 내려가는 것을 확인했다. 결국 ANG-TIE2 신호전달체계가 쉴렘관의 항상성을 유지함으로써 안압을 조절해 녹내장이 발병하지 않도록 하는 것이다. 이번 연구는 녹내장을 근본적으로 해결할 수 있는 치료법 개발에 큰 도움이 될 것으로 보인다. 특히 녹내장을 재현한 질병 모델에 TIE2 활성 항체를 주사해 안압 하강 효과를 얻은 만큼 추후 임상 연구로의 확장이 기대된다. 연구진은 방수배출장치의 또 다른 요소인 섬유주와 ANG-TIE2 신호전달체계의 관계를 밝히는 실험과 실제 환자에게 TIE2 활성 항체를 사용할 수 있을지 전임상 실험을 계획 중이다. 연구를 이끈 고규영 단장은 “이번 논문에는 이십여 개에 달하는 연구 이미지 세트가 실렸다. 일반적인 경우의 두 배에 달한다”며 “쉴렘관 항상성 유지의 기전을 자세히 밝히는 방대한 양의 연구를 수행했음을 보여준다”라고 말했다. 이번 연구결과는 미국 임상연구학회에서 발간하는 임상연구학회지(The Journal of Clinical Investigation, if 12.784)에 9월 19일 새벽 5시(한국시간)에 온라인판에 게재됐다. 또한 10월 발간되는 인쇄본의 표지 및 커버스토리로 실린다.
1) 쉴렘관(Schlemm’s canal): 독일의 해부학자 쉴렘이 발견한 쉴렘관은 방수가 정맥 속으로 흘러가는 통로이다. 쉴렘관은 혈관과 림프관의 중간 형태로 방수가 혈관을 통해 전신 순환계로 빠질 수 있게 돕는다. 눈의 모양체에서는 방수가 계속 생성되어 눈의 형태를 유지하고 각막과 수정체에 영양을 공급한다. 2) Angiopoietin-TIE2 신호전달체계: Angiopoietin과 TIE2 수용체는 혈관 성숙과 안정화를 조절하는 주요인자다. 혈관내피세포에 특이적으로 작용하여 혈관신생, 림프관신생, 조직수분 항상성 유지 및 혈관의 투과성, 염증 등을 조절하는데 매우 핵심적인 역할을 수행한다. 3) 방수: 눈 속에 차 있는 체액인 방수는 안압 유지와 안구 형성에 중요하다. 방수는 생성되는 만큼 홍채 가장자리에 위치한 섬유주와 쉴렘관으로 빠져나가 혈관을 통해 눈 밖으로 배출되어야 안압이 상승하지 않고 일정하게 유지된다. 4) Prox1 전사인자: Prox1 전사인자(prospero homeobox protein 1)는 림프관 내피세포의 특성을 결정하는 가장 중요한 조절 기능을 수행한다. 5) 거대액포: 쉴렘관 내벽에 위치해있으며, 방수가 이동하는 통로의 역할을 한다. 6) ERK: 인산화효소의 일종으로, TIE2가 활성화되면 뒤이어서 활성화되어 Prox1 전사인자의 발현을 증가시킨다. 7) Klf4: 전사인자의 일종으로, 전단응력(관의 내부를 호르는 액체가 관의 내벽에 작용하는 힘)에 반응하여 발현이 증가된다. |
|||
|
|
|||
| 다음 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 커뮤니케이션팀 : 권예슬 042-878-8237
- 최종수정일 2023-11-28 14:20