 뉴스센터
뉴스센터
죽어야 사는 세포의 운명- 세포의 일생-분열과 노화, 죽음에 이르기까지의 여정 -
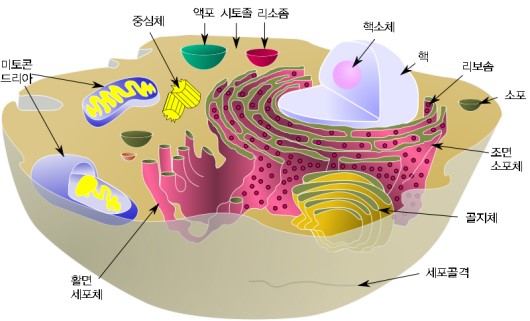
당신은 '생물'인가? 누구나 간단히 '그렇다'고 대답할 것이다. 그럼, 질문을 바꿔보자. 당신이 생물이라는 증거는 무엇인가, 당신이 무생물과 다른 점은 무엇인가? 많은 이들이 '숨을 쉬고 있다', '심장이 뛴다', '의식이 있다' 등등의 답을 할 지 모른다. 모두 일리가 있지만, 과학적으로 생물, 즉 생명체가 무생물과 구분되는 특징은 대략 다음과 같다. 자라서 유전과 증식(reproduction)을 한다, 물질대사(metabolism)를 통해 살아갈 에너지를 얻으며 스스로 생명을 유지한다, 환경에 대해 반응(response)하고 적응한다, 세대를 거치며 유전자를 변화시켜 천천히 진화(evolution)한다.인간은 이 모든 조건을 만족시키므로 생물, 즉 '생명체'라고 할 수 있다.' 세포는 위에 언급한 생명체의 특성을 모두 가지고 있는 가장 작은 단위다. 세포 분열을 통해 수를 늘리고(reproduction), 필요한 물질을 합성하거나 영양분을 분해하여 활동에 필요한 에너지를 만들고(metabolism), 주위 환경에 반응하며(response), 오랜 세월을 통해 유전자를 변화시켜 나가는(evolution) 존재인 것이다. 지구상에는 아메바처럼 단 한 개의 세포로 이루어진 생물도 있고, 인간처럼 수십~수백 조 개의 세포로 이루어진 생물도 있다. 많은 세포로 이루어진 생물의 경우 비슷한 기능을 가진 세포가 모여 조직을 만들고(상피 조직, 결합 조직, 근육 조직, 신경 조직 등), 조직이 모여 기관을(허파, 심장, 간, 대장, 소장, 혈관, 이자 등), 기관이 모여 기관계(소화계, 신경계, 호흡계, 순환계 등)를 이루어 비로소 하나의 생명체를 완성하게 된다.1)
세포를 목격한 사람들이번엔 사람이 세포로 이루어져 있다는 증거에 대해 이야기해 보자. 알다시피 당장 맨 눈으로 내 몸의 세포를 관찰하려고 해봤자 불가능하다. 인체 세포의 경우 평균 크기가 100 마이크로미터 정도 밖에 되지 않을 정도로 작기 때문이다.2) 이렇게 작은 세포의 존재를 처음 확인한 것은 1665년 영국 과학자 로버트 훅(Robert Hooke,1635~1703)이다. 왕립학회 실험 관리자였던 그는 직접 만든 현미경의 성능을 자랑하고 싶어 이것저것 관찰하던 중, 얇게 자른 코르크에서 칸막이로 나뉘어진 작고 텅 빈 공간이 빽빽이 들어차 있는 것을 발견하고 세포(cell)라는 이름을 붙였다.3) 그러나 세포가 모든 생물의 기본 단위라는 '세포설'이 등장한 것은 그로부터 한참 후였다. 1838년, 독일의 식물학자 마티아스 슐라이덴과 독일의 생리학자 테오도르 슈반이 각종 동물과 식물을 현미경으로 관찰한 끝에 '모든 생물체는 세포로 이루어져 있으며 세포에서 가장 기본적인 생명활동이 일어난다'고 주장한 것이다. 여기에 1858년 독일의 생리학자 루돌프 피르호(Rudolf Virchow, 1821~1902)가 '모든 세포는 세포로부터 탄생한다'는 주장을 덧붙여 세포설이 완성된다.
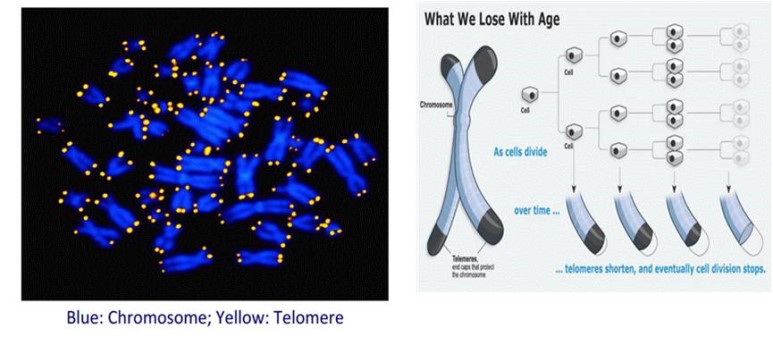
세포의 생로병사에 관하여세포도 생명체인 만큼 태어나고, 늙고, 죽는다. 모세포의 분열을 통해 태어난 세포는 다시 분열을 하여 새로운 세포를 낳는다. 새 세포는 수명을 다해 죽은 세포의 자리를 대신하게 된다. 위장 내벽 세포는 2시간 반 정도면 살다가 죽어 새로운 세포에게 자리를 내주고 적혈구는 3개월을 살고 교체된다. 신경 세포는 한번 출생 다음 해부터 더 이상 분열하지 않지만 간세포는 성장이 끝난 이후에는 분열을 멈추었다가 간의 일부가 파괴되었을 때 다시 분열을 시작하여 없어진 부분을 보충한다. 그러나 대부분의 인간 체세포는 25~30일 정도 살며 1년 정도면 몸에 있는 거의 대부분의 낡은 세포는 죽어 없어지고 새 세포로 교체된다. 1961년 해부학자 레너드 헤이플릭(Leonard Hayflick, 1928~)은 세포가 보통 70번 정도 분열을 하면 더 이상 분열하지 못한다는 것을 발견하고 '헤이플릭 한계'라 이름 붙였다, 1980년대 분자생물학자 엘리자베스 블랙번(Elizabeth Blckburn,1948~)은 그 이유가 세포의 염색체에 양 끝의 텔로미어(telomere)4)와 관계있다는 것을 밝혔다.4) 텔로미어는 염색체를 보호하기 위해 양 끝에 특정한 염기가 수천 번 반복되어 생긴 뚜껑 같은 부분인데, 세포가 분열할수록 점점 닳아서 짧아진다. 결국 텔로미어가 너무 짧아지면 세포는 더 이상 분열할 수 없게 된다.5) 이처럼 더 이상 분열하지 못하는 세포를 '노화'되었다'한다. 노화된 세포는 일단 크고 평평해 지며, 유전자 발현이 잘 되지 않고 갖가지 노화 관련 질병에 영향을 주는 물질을 분비하기도 한다. 이로 인해 개체는 동맥경화, 감각기관 기능저하, 상처회복 및 면역능력 약화 등을 겪게 되는 것이다. 개체의 노화 현상에는 세포 차원의 노화 외에도 많은 이유가 있는 것으로 알려졌지만, 전반적인 세포의 노화도 큰 상관관계가 있는 것을 알려졌다.
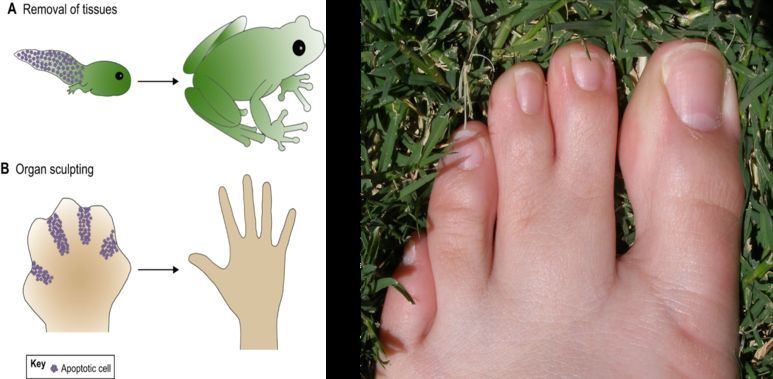
세포의 죽음은 크게 아폽토시스(apoptosis)와 네크로시스(necrosis) 둘로 나눌 수 있다. 네크로시스를 괴사, 아폽토시스를 사멸이라고도 한다. 네크로시스는 심한 충격이나 방사선, 독극물 등의 외부 스트레스에 의해 세포가 괴사하는 것을 말한다. 가구 모서리에 다리를 부딪쳐 타박상이 드는 것도 세포의 네크로시스 때문이다. 네크로시스가 일어나면 세포는 팽창하면서 녹아내리고 여기에 백혈구가 모여서 염증 반응이 일어난다. 아폽토시스는 사고사가 아닌 정해진 운명에 의해 일어나는 죽음이다. 세포가 수명을 다하거나 필요 없어지면 저절로 죽어 없어지는 것도 사멸의 과정이다. 올챙이의 꼬리가 없어지는 것, 물갈퀴가 달린 개구리 발처럼 이어져 있던 태아의 손가락이 하나하나 분리되는 것이 바로 세포의 아폽토시스 때문이다.
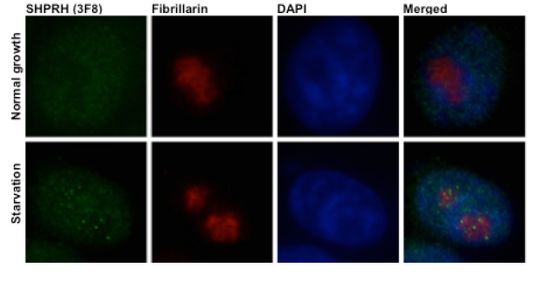
아폽토시스는 외부 스트레스 때문에 세포가 크게 손상되었을 때도 실행된다. 방사선이나 바이러스 감염, 화학약품, 활성산소 등으로부터 공격을 받아 손상된 세포는 일단 고치는 것을 시도한다. 그러나 그 손상이 너무 크면, 복구보다는 세포를 모두 없애고 정상 세포를 증식하는 플랜 B를 작동시키는 것이다. 아폽토시스로 쪼그라들고 쪼개진 세포의 시체는 면역 세포의 하나인 대식 세포가 먹어치운다. 이 과정이 제대로 작동하지 않으면 손상된 세포는 좀비 세포가 되어 정상세포로 갈 영양소까지 모두 빨아들이며 무섭게 커져 결국은 개체의 생명도 위협한다. 암이나 자가면역질환, AIDS, 알츠하이머 등이 그것이다. 결국 세포는 죽어야 산다는 아이러니한 메커니즘을 가진 셈이다. 오래 살고 싶다면 세포 다이어트그렇다면 텔로미어가 짧아지지 않게 하여 개체의 노화를 막을 수도 있지 않을까? 존스홉킨스대 캐럴 그라이더 교수는 텔로미어를 짧아지지 않게 해 주는 효소를 발견해 엘리자베스 블랙번 교수와 함께 노벨상을 받았다. 캐럴 그라인더 교수는 대부분의 암세포가 아무리 분열을 많이 해도 텔로미어가 짧아지지 않는데 주목했고, 그것이 텔로미어를 만드는 데 관여하는 텔로머라제(telomerase)라는 효소 때문임을 밝혀냈다. 현재 이 텔로머라제를 이용하여 노화와 암 증식을 막을 수 있는 방법이 연구되고 있다. 이 외에도 세포 차원에서 노화를 막아보고자 하는 노력은 전 세계에서 다양하게 진행되고 있다. 장수와 관련된 유전자에 관한 연구나 미토콘드리아에서 에너지를 만들 때 만들어져 생물체를 늙게 만든다는 활성 산소에 대한 연구 등이 그것이다. 우리나라에서도 최근 관련 연구 성과들이 속속 보고되고 있다. 명경재 단장이 이끄는 IBS 유전체 항상성 연구단은 지난 4월 SHPRH라는 단백질이 노화와 암 진행을 막는 데 큰 역할을 한다는 새로운 사실을 밝혀냈다. SHPRH는 원래 손상된 DNA를 고치는 단백질인데, 망가진 DNA가 없을 때는 엠토(mTOR;mammalian target of rapamycin)6)라는 대사 경로에 작용해 노화와 암 진행을 늦춘다는 것이다. mTOR 대사는 세포의 영양분이 부족할 때 리보솜 DNA의 전사를 억제하는 방식으로 이루어진다. 즉, 리보솜 DNA를 RNA로 전사할 때는 SHPRH 단백질이 DNA 프로모터와 결합하고, 그것이 다시 RNA 중합효소와 결합하는데, 세포내 영양분이 부족해지면 SHPRH 단백질들이 뭉치면서 결합을 막는다는 것이다. 때문에 단백질 합성 공장인 리보솜이 덜 만들어지고, 결국 단백질 생산이 줄어들어 노화와 암진행도 느려진다는 것이다.
또한 IBS 식물 노화․ 수명 연구단(단장 남홍길)은 지난 3월, 포스텍 연구팀과 공동으로 그 동안엔 알려지지 않았던 RNA와 노화의 상관관계를 밝혀내기도 했다. 즉, 나이가 들면 RNA도 많은 손상을 입으므로 RNA를 최적의 상태로 유지하면 노화도 늦츨 수 있다는 것이다. RNA를 최적의 상태로 유지하는 데는 기능이 떨어지거나 비정상적으로 생성된 RNA를 제거하는 NMD(nonsense-mediated mRNA decay) 현상에 의해 이뤄진다. 연구팀은 특별히 오래 사는 예쁜꼬마선충을 관찰한 결과 노화해도 NMD 작용이 활발해짐을 밝혔으며, 특히 신경세포 내의 NMD 작용을 활성화하는 것이 수명 연장에 매우 중요하다는 결과를 얻었다. 2천 여 년 전 진시황은 불로불사의 약을 얻기 위해 신하들을 전 세계 곳곳으로 보냈다고 한다. 현대 과학은 머지않아 그 비밀을 실험실의 작디작은 세포 속에서 발견할 지도 모른다. 1) 식물은 세포-조직-조직계-기관-개체 2) 1 마이크로미터(㎛)는 1cm를 만 번 나눈 것 중의 하나. 그러니 우리 몸의 세포는 보통 1백분의 1 cm정도의 크기다. 크기가 비교적 큰 세포도 있긴 하다. 달걀, 메추리알, 개구리알과 같은 동물의 알이 그것이다. 가장 큰 알을 낳는 지구상의 동물은 타조이므로 타조알은 크기가 십여 cm나 되는 세상에서 가장 큰 세포가 된다. 3) 사실 이것은 세포가 아니라 죽은 세포의 껍데기(세포벽)일 뿐이었다. 실제 살아있는 세포를 관찰한 것은 네덜란드 과학자 안토니 판 레이우엔훅(Antonie van Leeuwenhoek,1632~1723)이다. 4) 캘리포니아대학 교수인 엘리자베스 블랙번과 하버드 의대 조스택 교수는 텔로미어에 관한 연구의 공로로 2009년 노벨 생리의학상을 받았다. 5) 모든 세포가 '헤이플릭한계'를 갖는 것은 아니다. 생식세포나 혈구를 생산하는 조혈모세포 등은 분열을 거듭해도 텔로미어가 짧아지지 않아 계속해서 분열할 수 있다. 6) 포유동물에 존재하는 세린/트리오닌 단백질의 인산화 효소다. 세포의 성장과 증식, 운동성, 생존, 단백질 합성, 전사를 조절한다. 본 콘텐츠는 IBS 공식 블로그에 게재되며, blog.naver.com/ibs_official/ 에서 확인하실 수 있습니다. |
| 다음 | |
|---|---|
| 다음 |
- 콘텐츠담당자
- 홍보팀 : 임지엽 042-878-8173
- 최종수정일 2023-11-28 14:20