 뉴스센터
뉴스센터
시냅스 조절하는 핵심단백질 구조 최초 규명- 자폐증 등 뇌정신질환 치료 적용 기대 -
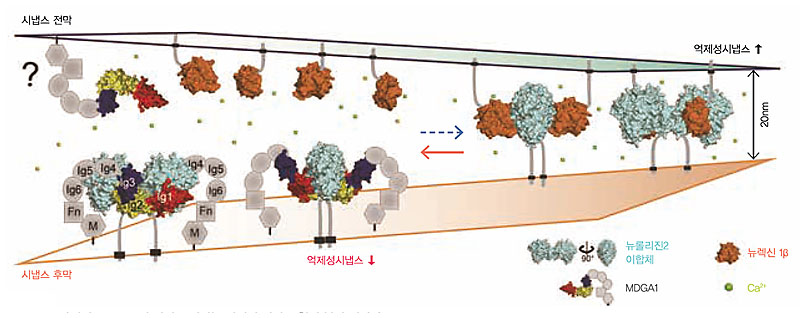
뇌는 생물체의 내·외부에서 들어오는 모든 정보를 통합하고 처리해 생명유지에 필수적인 기능과 행동을 조절하며 학습과 기억능력도 담당한다. 이런 기능을 수행하기 위해 뇌는 매우 많은 신경세포로 이루어져 있다. 신경세포는 두 신경 세포가 연접하면서 형성되는 시냅스(synapse)를 통해 기능에 맞는 신호를 전달한다. 시냅스는 뇌 활동에 필요한 기본 단위다. 시냅스의 종류로는 흥분성 시냅스(excitatory synapse)와 억제성 시냅스(inhibitory synapse)가 있다. 흥분성 시냅스는 신경세포 사이의 접합이 계속 일어나 다른 신경세포를 흥분시키는 물질을 방출하는데 반해, 억제성 시냅스는 다른 신경세포의 흥분을 억제하는 물질을 방출한다. 두 시냅스는 서로 균형을 맞춰 신경전달이 효율적으로 일어나게 하는데, 이 균형이 깨질 경우 자폐증, 조울증을 포함한 다양한 뇌정신 질환이 발생할 수 있다. 시냅스 발달에는 시냅스 접착단백질이 관여한다. 대표적인 시냅스 접착단백질인 뉴롤리진(neuroligin)과 뉴렉신(neurexin)은 서로 결합해 흥분성 시냅스와 억제성 시냅스의 성장과 유지를 조절한다. 그러나 이 단백질들이 어떻게 결합하고 시냅스를 발달시키는지 그 구체적인 메커니즘은 명확히 밝혀지지 않았다. IBS 시냅스 뇌질환 연구단 김은준 연구단장·카이스트 김호민 교수·대구경북과학기술원(DGIST) 고재원 교수 연구팀은 뉴롤리진과 뉴렉신의 결합을 조절한다고 알려진 'MDGA1'이라는 시냅스 내 단백질의 3차원 구조를 밝히고, MDGA1이 억제성 시냅스 형성을 저해하는 메커니즘을 최초로 규명했다. 억제성 시냅스 조절 기능이 망가지면 뇌의 흥분성이 급격히 증가한다. 그러면 이와 관련된 시냅스와 신경회로 활성에 이상이 생겨 뇌질환이 발병할 위험도 커진다. 이번 연구로 흥분성 시냅스와 억제성 시냅스의 균형 이상으로 생기는 다양한 정신질환의 발병하는 원인을 분자 수준에서 이해 할 수 있는 길이 열렸다.
연구팀은 먼저 단백질 결정학 방법을 활용해 MDGA1 단백질 복합체 및 MDGA1와 선택적으로 결합한다고 알려진 단백질, 뉴롤리진―2를 결정화하고 3차원 구조를 분석했다. MDGA1은 후시냅스의 단백질로, 연구팀은 이 단백질이 뉴렉신과 뉴롤리진-2 사이의 결합을 방해하고 뉴렉신보다 뉴롤리진-2에 더 경쟁적으로 결합함으로써 억제성 시냅스 형성을 저해한다는 사실을 발견했다. 뉴롤리진과의 결합 면에서 MOCA1가 뉴렉신보다 더 우세한 것이다. 연구팀은 생쥐를 이용한 실험에서도 MDGA1이 억제성 시냅스에 존재하는 뉴롤리진-2에만 선택적으로 결합해 억제성 시냅스 발달을 조절한다는 점을 입증했다. 포유류에는 크게 네 가지 종류의 뉴롤리진 유전자(neuroligin-1, neuroligin-2, neuroligin-3, neuroligin-4)와 두 가지 종류의 MDGA 유전자(MDGA1, MDGA2)가 존재한다. 실험 결과 생화학적으로는 MDGA1과 MDGA2가 뉴롤리진-1과 뉴롤리진-2에 비선택적으로 결합하지만, 실제 생쥐의 뇌 속에서는 알려지지 않은 메커니즘에 의해 MDGA1이 뉴롤리진-2에만 선택적으로 결합해 억제성 시냅스 발달을 억제한다는 사실을 보여줬다. 김호민 교수는 "이번 연구 성과는 단백질 구조 생물학과 신경생물학의 유기적인 협력 연구를 통해 시냅스 발달 조절에 핵심적인 MDGA1의 구조와 작용 메커니즘을 최초로 규명했다는 의의가 있다"라며 "이로써 시냅스 단백질들의 기능 이상으로 나타나는 다양한 뇌정신질환의 발병 메커니즘을 폭넓게 이해할 수 있을 것이다" 라고 말했다. 이번 연구는 시냅스 형성 억제에 관여하는 MDGA1과 대표적인 시냅스 접착단백질인 뉴롤리진-뉴렉신의 새로운 분자적 작동 메커니즘을 제시해 시냅스 조절 단백질(synaptic regulation molecules) 연구를 선도할 것으로 기대된다. 김호민 교수는 "향후 흥분성 및 억제성 시냅스에서 일어나는 추가적인 단백질 결합과 구조에 관한 연구를 진행할 것"이며 "궁극적으로는 자폐, 정신분열증 등의 정신질환을 치료하는 약물을 개발하는 데까지 나아갈 것"이라고 전망했다. |
|||
Center for Synaptic Brain Dysfunctions (시냅스 뇌질환 연구단)Publication Repository |
| 이전 | |
|---|---|
| 이전 |
- 콘텐츠담당자
- 홍보팀 : 임지엽 042-878-8173
- 최종수정일 2023-11-28 14:20